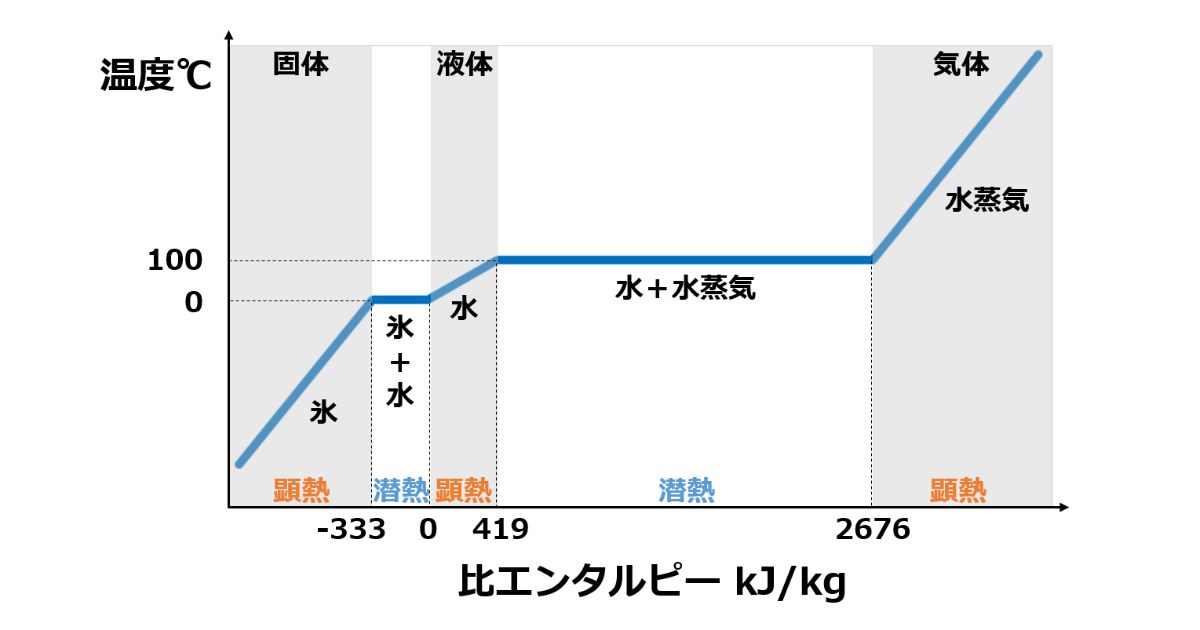
蒸留は、混合物をその揮発性の差を利用して分離・精製する基本的な単位操作の一つです。
工業的には、用途に応じて様々な蒸留法が考案されています。
- 基本的な蒸留
- 単蒸留:一番単純な蒸留機構だが純度は低い
- 精留:単蒸留を繰り返して純度を上げたもの
- 圧力操作による蒸留
- 減圧蒸留:減圧により物質の沸点を下げて蒸留
- 分子蒸留:減圧蒸留よりも高真空での蒸留
- 加圧蒸留:沸点が低い物質を加圧して蒸留
- フラッシュ蒸留:連続的に単蒸留を行う
- 特殊な蒸留
- 反応蒸留:反応系中の成分を蒸留しながら反応する
- 水蒸気蒸留:水蒸気とともに高沸点成分を蒸留
- 抽出蒸留:沸点が近い2成分に第3成分を加えることで蒸留分離可能にする
- 膜蒸留:気体だけを透過する多孔質膜で分離する
基本的な蒸留
まずは基本的な蒸留操作について解説します。
単蒸留
単蒸留は、最もシンプルな蒸留方法であり、小学校から高校までの教育課程でも紹介される基本的な手法です。
容器内の液を加熱し蒸発させ、冷却した蒸発分を分取することで低沸点成分の比率が高い液を得られます。
分離能はそれほど高くないため、純度を求めた分離には向きません。
原料が少ない場合、不揮発性成分との分離の場合、沸点に大きな差がある場合などで利用されます。
例えば海水から水だけを蒸留で取り出す場合は単蒸留でも構いません。
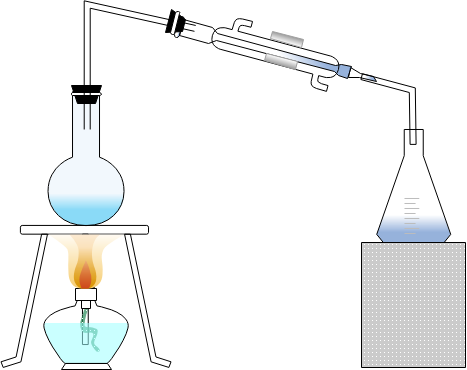
精留:蒸留塔
単蒸留は分離能が良くないですが、蒸留物を更に蒸留して、その蒸留物を更に蒸留……と単蒸留を繰り返すことで純度を上げることができます。
これを精留と呼びます。
ただし、工業的に何度も単蒸留を繰り返すのは非効率的でコストも高くなります。
これを解決するために考案されたのが蒸留塔です。
1本の塔の中で蒸留するだけで単蒸留を何度も繰り返したような効果が得られる構造となっています。
効率的に純度の高い蒸留効果を得たい場合や沸点にそれほど差がない場合に利用されます。

単蒸留から蒸留塔へスケールアップするイメージは以下の記事を参考にしてください。
圧力操作を伴う蒸留
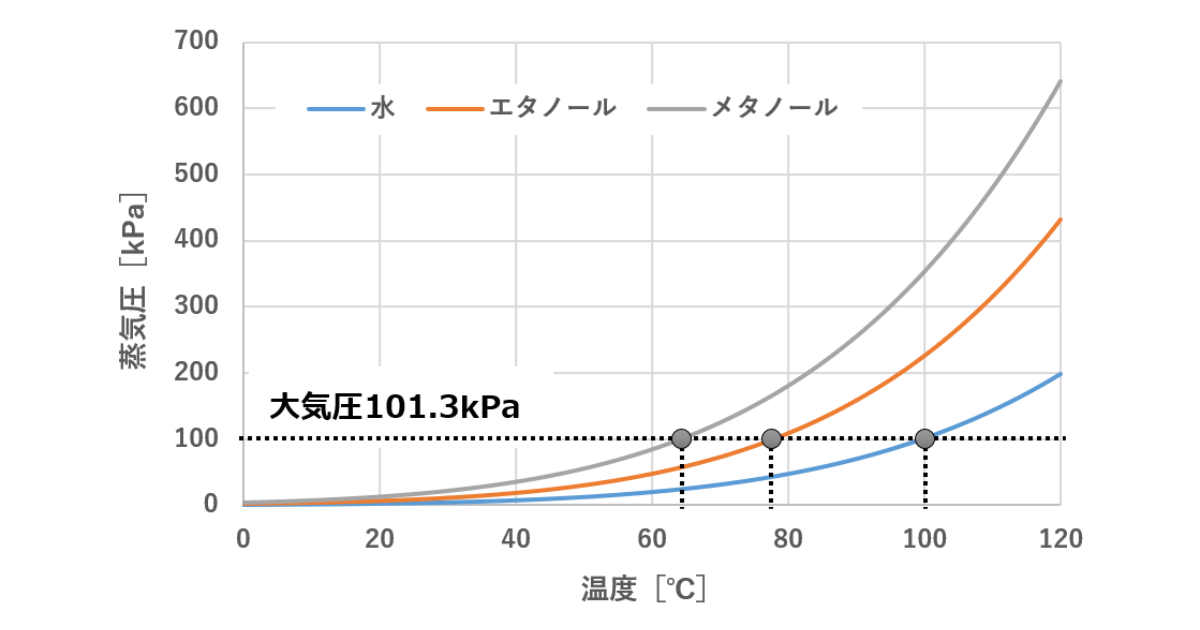
蒸留は物質の沸点を利用するため、圧力と密接に関わります。
物質の多くは、圧力が上がると沸点は上がり、圧力が下がると沸点は下がります。
圧力を操作することで、常圧では難しい分離を可能にします。
減圧蒸留
加熱が必要な蒸留工程において、減圧した状態で蒸留することで沸点を下げ、加熱温度を下げることができます。
減圧蒸留は主に以下の条件において活躍します。
- 高温での加熱により分解・重合する物質
- 酸化する物質
- 沸点が異常に高い物質
- 減圧にすることで共沸点がなくなる場合
例えば、高沸点の有機化合物の精製や天然物からの芳香成分の抽出などが挙げられます。
ただし真空ポンプや減圧装置が必要であり、設備投資が増加します。
加圧蒸留
沸点が非常に低い物質を利用する場合、減圧蒸留とは対照的に加圧蒸留する場合もあります。
冷却媒体を必要温度まで下げられず蒸発物質を凝縮しきれない場合に有用です。
フラッシュ蒸留
フラッシュ蒸留は連続蒸留の中で最も単純な蒸留です。
液体を減圧下に急速に送り込むことで、蒸留ドラム内で気液平衡が瞬間的に形成され、2成分に分離できます。
フラッシュ蒸留は連続蒸留であることから粗く大量に処理することができます。
また単一段での気液平衡を利用するため、設備が簡素です。
特殊な蒸留
通常の蒸留では分離できない場合に利用される特殊な蒸留手法も存在します。
使用頻度は比較的少なくなります。
分子蒸留
分子蒸留は、減圧蒸留よりもさらに高い真空度で蒸留します。
蒸発する分子が液体の表面から飛び出した際に、気体分同士が衝突せずにそのまま移動できるような高い真空条件で行われます。
つまり、蒸発した気体は全て凝縮・分離できるため非平衡状態で蒸留が行われることを意味します。
この時の蒸発速度は、蒸気圧が高く、分子量が小さいほど早くなります。
高真空で基本的に蒸気圧が低い状態で実施することから蒸発速度は小さく、液を薄膜上にして蒸留する方式(流下膜・遠心膜)がとられます。
熱に非常に敏感な物質の熱劣化を最小限に抑えたい場合に適しています。
反応蒸留
反応蒸留では、蒸留と化学反応を同一装置内で同時に行います。
平衡制限反応の平衡をシフトさせることで、反応率を高めることが可能です。
例えばエステル化反応は系内の水を取り除くことで平衡が生成物側に偏るため、反応蒸留の方式がとられます。
エステル化の場合は取り除いた水の量から反応率が計算できることから、反応の進捗を予測することも可能です。
水蒸気蒸留
水蒸気蒸留は水蒸気を蒸留塔へ吹き込みながら、水蒸気とともに蒸発させます。
塔内の水蒸気の分圧が上がることで、目的物質の蒸気分圧が下がり蒸発温度を低くします。
また水蒸気は直接加熱源としても利用されます。
凝縮物は水との2層を形成するため、水を分離精製すれば目的成分が得られます。
蒸留の温度を下げられるメリットはありますが水に不溶な物質でなければなりません。
抽出蒸留
抽出蒸留では、2成分の沸点が近い場合や共沸する場合に第3成分を加えることで蒸留を可能にします。
添加により2原料間の比揮発度を大きくすることが目的です。
ここで添加する第3成分はエントレーナーとも呼ばれます。
第3成分は沸点が原料よりも高く溶解性があることが条件です。
工業的にはブタジエンやイソプレンの抽出蒸留が有名で、溶剤にはDMFが使用されます。
-
-
ブタジエンやイソプレンの抽出蒸留
www.zeon.co.jp
膜蒸留
膜蒸留は、蒸気だけを透過する多孔質膜を介して蒸気圧差により揮発性成分を分離する方法です。
主に水処理分野で使用されています。
原理的には通常の蒸留と変わりませんが膜を介して分離している点で膜分離に分類されるかもしれません。
水処理分野において、高いエネルギーや広いスペースを用いないことから活用されています。
-
-
膜蒸留法に適した高耐水圧PTFE多孔質 中空糸膜
sumitomoelectric.com
オススメ書籍
・トコトンやさしい蒸留の本
蒸留を勉強するときに最初に読んでおきたい書籍です。
国内の蒸留研究で有名な大江先生が書かれています。
-

-
トコトンやさしい蒸留の本
www.amazon.co.jp
・絵とき「蒸留技術」基礎のきそ
「トコトンやさしい蒸留の本」で蒸留の考え方に慣れてきたらこちらの本でステップアップします。
様々な条件における蒸留計算が体系的に解説されています。
-

-
絵とき「蒸留技術」基礎のきそ
www.amazon.co.jp
・化学工学ー解説と演習ー
化学工学を勉強したい!と思ったら真っ先にオススメしたい書籍です。
蒸留に関しては装置構成についても触れられています。
また、他の汎用化学工学書籍には無い「撹拌動力計算」や「撹拌伝熱計算」も記載されています。
-

-
化学工学―解説と演習ー
www.amazon.co.jp