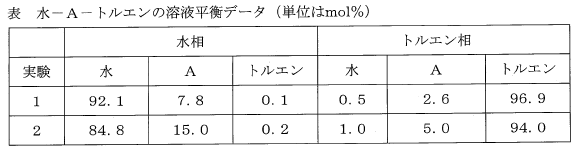
水100 molに成分Aを20 mol溶解した水溶液がある。これに、純粋なトルエン100 molを加え、容器の中で撹拌し、静置したところ、2液相に分離した。上層に含まれる成分Aの量として、最も近い値はどれか。水とトルエンの相互溶解度は無視できる。溶液平衡の実験データを下表に示す。
根の公式は次の通りである。
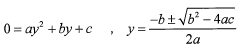
- 16 mol
- 5.2 mol
- 5.0 mol
- 4.6 mol
- 4.0 mol
解答解説
正答は4番です。
水の比重よりトルエンの比重の方が小さいことから、上層がトルエン、下層が水となります。
今回、成分A濃度の異なる液液平衡データが2種類与えられています。それぞれで分配係数を計算してみます。希薄溶液であり、抽出により分子が変化しない場合は分配係数が同じになります。
1行目:2.6 / 7.8=1/3
2行目:5.0 / 15.0=1/3
分配係数が1/3ですので、各層におけるAのモル分率xwaterとytolから立式します。上層であるトルエン相の成分Aの物質量はnAとします。使用する成分Aは20 molですので、水相側の成分Aの物質量は(20-nA)です。
xwater=(20-nA) / {100+(20-nA)}
ytol=nA / (100+nA)
上記式からytol=1/3 xwaterを立式してnAを求めます。
nA / (100+nA)=1/3 × (20-nA) / {100+(20-nA)}
nA2 - 220nA+1000=0
根の公式(解の公式)よりnA=110±10√(111)です。√(111)≒10.54とすると、110 ± 10 × 10.54=4.6もしくは215.4 molとなります。使用している成分Aは20 molですので、必ず20 mol以下になります。
よって最も近いのは4.6 molです。


