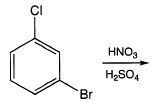
m-ブロモクロロベンゼンをニトロ化した。主生成物として、最も生成量が多いものは、次のうちのどれか。
- 2-ブロモ-4ークロロ-1, 3, 5-トリニトロベンゼン
- 1-ブロモ-3-クロロ-2-ニトロベンゼン
- 4-ブロモ-2-クロロ-1-ニトロベンゼン
- 2-ブロモ-4-クロロ-1-ニトロベンゼン
- 1-ブロモ-3-クロロ-2, 4-ジニトロベンゼン
解答解説
正答は4番です。
ニトロ化は硝酸と硫酸の混酸系中で生成するニトロニウムイオン(NO2+)が活性種として作用します。ニトロ基自体が電子求引性の不活性基であるため反応性が低下します。よって通常はモノニトロ化で反応は停止します。
ブロモ基とクロロ基どちらもオルト-パラ配向性を示します。またニトロ基はメタ配向性を示します。配向性を考えると、この時点ではベンゼン環の臭素原子を基準に2, 4, 6位全ての箇所へニトロ基が結合する可能性があります。
この反応で注目するのは電気陰性度です。炭素が2.6、臭素が3.0、塩素が3.2です。つまり炭素-臭素結合や炭素-塩素結合において、炭素原子側はδ+に偏ります。それは電気陰性度の大きな炭素-塩素結合の方が偏りが大きくなります。
活性種としてニトロニウムイオン(NO2+)が作用することから、δ+性の低い炭素原子で反応が起こりやすいことを意味します。よって臭素原子に隣り合う炭素、中でも塩素原子と遠い側の炭素において反応が起きやすくなります。
参考資料
-
-
芳香族化合物のニトロ化
www.chem-station.com
-
-
「芳香族求電子置換反応 (2)
www1.meijo-u.ac.jp
-
-
電気陰性度
www.try-it.jp


