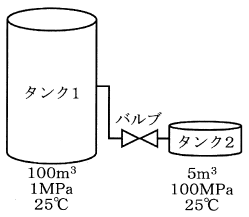
閉じたバルブにより接続された大小2基のタンクがある。100 m3のタンク1には1 MPaの気体が充填されており、5 m3のタンク2には100 MPaの気体が充填されている。気体は共に同じ理想気体であり、温度は共に25℃である。閉じていたバルブを開けて、2基のタンク内の圧力を均一とした場合の圧力として、最も適切な値はどれか。
断熱膨張による温度変化は考慮せず、25℃一定とする。
また、気体の状態方程式はPV=nRTであり、Pは圧力(Pa)、Vは容積(m3)、nは気体の物質量(mol)、Rは気体定数(Jmol-1K-1)、Tは気体の温度(K)である。
- 5.5 MPa
- 5.7 MPa
- 5.9 MPa
- 6.1 MPa
- 6.3 MPa
解答解説
正答は2番です。
バルブを開けた時、全体の体積Vは100+5=105 m3です。また25℃の時の絶対温度Tは25+273=298Kです。
理想気体の状態方程式PV=nRTより、各タンク内に含まれる気体の分子量はn=PV/RTを計算すれば求まります。バルブを開けた後は、各タンクの分子量を合計した値となります。
- タンク1の気体の分子量n1:1×106×100/(R×298)
- タンク2の気体の分子量n2:100×106×5/(R×298)
理想気体の状態方程式より、バルブを開けた後の圧力Pは(n1+n2)RT/Vで計算できます。計算量が複雑に見えますが、MPaへの変換のために106は計算せず残しておくことが可能で、(R×298)は約分して消せます。
P=nRT/V={1×106×100/(R×298)+100×106×5/(R×298)}×R×298 / 105 = 600/105 MPa = 5.7 MPa


