次の3つの化合物A~Cのルイス構造を記したとき、カッコ内に示した元素の形式電荷の組合せとして、最も適切なものはどれか。ただし、ルイス構造では8電子則が常に満たされているものとする。
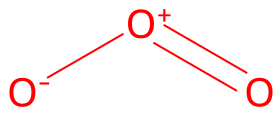
- オゾンO3(中心の酸素O)(構造は非環状の曲がった形状)
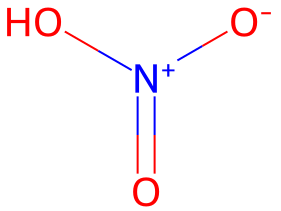
- 硝酸HO-NO2(窒素N)
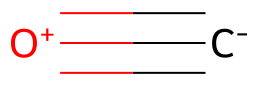
- 一酸化炭素CO(酸素)
| 選択肢 | A | B | C |
|---|---|---|---|
| 1 | -1 | +1 | +1 |
| 2 | -1 | -1 | +1 |
| 3 | +1 | +1 | -1 |
| 4 | +1 | -1 | +1 |
| 5 | +1 | +1 | +1 |
解答解説
正答は5番です。
オゾンはO=O+-O-という結合をしています。つまり中心の酸素Oの形式電荷は+1です。
硝酸はN+に-OH、-O-、=Oが結合しています。つまり窒素Nの型式電荷は+1です。
一酸化炭素はC-とO+が三重結合で結合しています。つまり酸素Oの形式電荷は+1です。
参考資料
-
-
形式電化とは?
chemblogno1.blogspot.com


